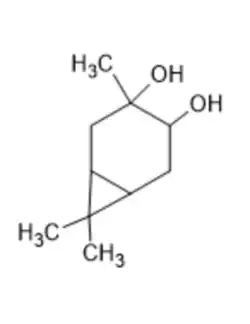
Carane-3,4-diol
| Carane-3,4-diol | |
| |
| Identification | |
|---|---|
| Nom UICPA | 3,7,7-Trimethylbicyclo[4.1.0]heptane-3,4-diol |
| Synonymes |
3,4-dihydroxycarane |
| PubChem | 8549 |
| SMILES | |
| InChI | |
| Propriétés chimiques | |
| Formule | C10H18O2 [Isomères] |
| Masse molaire[1] | 170,248 7 ± 0,009 9 g/mol C 70,55 %, H 10,66 %, O 18,8 %, |
| Propriétés physiques | |
| T° fusion | 177 °C |
| T° ébullition | 118,39 °C[2] |
| Point critique | 532,81 °C |
| Thermochimie | |
| ΔfH0gaz | −445,29 kJ·mol-1 |
| ΔfusH° | 14,62 kJ·mol-1 |
| ΔvapH° | 67,98 kJ·mol-1 |
| Unités du SI et CNTP, sauf indication contraire. | |
Le carane-3,4-diol est un composé organique appartenant à la classe des diols, de formule moléculaire C10H18O2. Il s’agit d’un dérivé hydroxylé du carane, possédant un noyau bicyclique substitué par deux groupes hydroxyles en positions 3 et 4[3]. Le carane-3,4-diol est utilisé dans les formulations herbicides et pesticides[4], améliorant ainsi leur efficacité. Il a également été étudié pour son activité herbicide, en particulier contre des espèces telles que le Lolium multiflorum et le Brassica campestris.
Synthèse du carane-3,4-diol
Dihydroxylation du 3-carene
La méthode la plus courante pour synthétiser le carane-3,4-diol est la dihydroxylation du 3-Carène. Plusieurs réactifs peuvent être utilisés : Une réaction possible utilise I₂ et AgOAc dans un solvant d’acide acétique[5]. Une autre variante utilise également I₂ mais remplace AgOAc par Hg(OAc)2 toujours dans un solvant d’acide acétique[6].

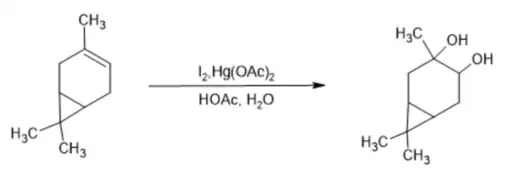
Une autre approche pour synthétiser le carane-3,4-diol repose sur l'utilisation de l'oxyde d'osmium(VIII) OsO4, en présence de TMAO (trimethylamine-N-oxide)[7]. La réaction se déroule dans un mélange eau/acétone sous reflux.
.png)
Cette réaction suit deux mécanismes principaux :
Syn addition : L'alcène réagit avec un agent oxydant métallique (exemple : OsO₄, dilute KMnO₄), formant un ester métallique cyclique (ester osmate ou manganate). L’hydrolyse de cet intermédiaire donne un diol où les deux groupes -OH sont ajoutés du même côté du plan moléculaire.
Anti addition : L'alcène est d'abord oxydé par un réactif électrophile. (exemple : I₂, Hg(OAc)₂), formant un intermédiaire halonium ou mercuronium cyclique. Cet intermédiaire est ensuite ouvert par l’eau via un mécanisme SN2, produisant un diol où les groupes -OH sont ajoutés de part et d’autre du plan moléculaire.
Applications et utilisation en tant que pesticide et herbicide
Le carane-3,4-diol est un composé bioactif avec de puissantes propriétés herbicide[8] et pesticide. Sa structure moléculaire lui permet de se dégrader rapidement dans l’environnement, ce qui en fait une alternative plus sûre et plus durable par rapport aux agrochimiques synthétiques. Le Carane-3,4-diol est préféré en raison de sa toxicité sélective et de sa biodégradabilité[9].Contrairement aux pesticides conventionnels qui persistent dans le sol et l'eau, le Carane-3,4-diol se décompose rapidement, minimisant les risques environnementaux. Sa forte solubilité permet une application facile sans solvants nocifs, réduisant ainsi les dangers pour les agriculteurs et les écosystèmes environnants. Le Carane-3,4-diol cible des mauvaises herbes comme Lolium multiflorum et Brassica campestris en endommageant les membranes cellulaires, et perturbant l'absorption des nutriments. Cela provoque un stress oxydatif, conduisant à une déshydratation et une inhibition de la croissance, permettant aux cultures de prospérer avec moins de concurrence pour les ressources. Le Carane-3,4-diol se dégrade naturellement, évitant l’accumulation de résidus toxiques dans le sol et l'eau. Ses fonctions herbicide et pesticide réduisent le besoin de traitements multiples, en faisant une solution rentable et écologique pour les agriculteurs. Les recherches en cours se concentrent sur l’optimisation des formulations de Carane-3,4-diol pour une stabilité et une efficacité accrues. Les scientifiques explorent également des synergies avec d'autres composés naturels pour améliorer son efficacité en agriculture durable.
Autres applications potentielles
Le carane-3,4-diol joue un rôle dans la production d'insecticides , tels que l'acide (1R)-trans-chrysanthemique, qui est un composant clé des pyréthrines, insecticides naturels extraits des fleurs de chrysanthème[10].
Pour obtenir l'acide (1R)-trans-chrysanthemique, l'utilisation du Carane-3,4-diol joue un rôle clé. Lorsque le Carane-3,4-diol réagit avec un ester, il conduit à la formation de l'acide trans-chrysanthemique. Après cette réaction, une hydrolyse et une séparation par chromatographie sur colonne permettent l'isolement des deux stéréoisomères, de l'acide (1S)-trans-chrysanthemique et de l'acide (1R)-trans-chrysanthemique[11]. L'acide (1R)-trans-chrysanthemique, essentiel à la préparation de certains insecticides, peut alors être récupéré. Ces deux isomères sont distinguables par leurs valeurs de Rf de 0,62 et 0,65, respectivement.
Sécurité et réglementation
L’utilisation du Carane-3,4-diol est sûre pour l’environnement car il est biodégradable[12]. Cependant, il existe des risques pour la santé humaine associés à son utilisation[13]. À fortes doses, il peut être irritant pour la peau et toxique. Il est également facilement métabolisé par de nombreuses enzymes présentes dans le foie, ce qui rend le carane-3,4-diol dangereux en cas d’ingestion.
Notes et références
- ↑ Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- ↑ « Chemical Properties of carane-3,4-diol », sur chemeo.com.
- ↑ « Caranediol », sur pubchem.ncbi.nlm.nih.gov.
- ↑ Huang Y, Zhu M, Lan H, Huang D, Lan M et Huang Y, Carane-3,4-diol Derivatives as Potential Water-Based Herbicides Chem Biodivers. 2024 Jun;21(6):e202301867., , Epub (PMID 38581645, DOI 10.1002/cbdv.202301867).
- ↑ Arbuzov, B.A., Isaeva, Z.G., D'yakonova, R.R. et Bakaleinik, G. A., β-cis-Hydroxylation of 3-carene, vol. 22, Bulletin of the Academy of Sciences of the USSR, Division of chemical science, (DOI https://doi.org/10.1007/BF00926400), p. 2483–2487.
- ↑ Arbuzov, B.A., Isaeva, Z.G., D'yakonova, R.R.V., Shaikhutdinov, A. et Kazakova, É. Kh., Synthesis of 3β,4β-caranediol., vol. 21, Bulletin of the Academy of Sciences of the USSR, Division of chemical science, (DOI https://doi.org/10.1007/BF00850554), p. 1634.
- ↑ Ta-Jung Lu et Cheng-Kun Lin, « Asymmetric Synthesis of α-Methyl-α-Amino Acids via Diastereoselective Alkylation of (1S)-(+)-3-Carene Derived Tricyclic Iminolactone », The Journal of Organic Chemistry, vol. 76/Issue 6, ?.
- ↑ ZHU Maomao, HUANG Yanqun, LU Pingping, HUANG Daozhan. Herbicidal Activity of Carane-3, 4-diol[J]. Biomass Chemical Engineering
- ↑ Application of carane-3, 4-diol as herbicide or in preparation of herbicide,HUANG DAOZHAN; ZHU MAOMAO; HUANG YANQUN; LAN HONGYUN; HE XUEWEI; LING MEIZHEN 黄道战; 朱茂茂; 黄焰群; 蓝虹云; 何雪薇; 凌妹珍; HUANG DAOZHAN; ZHU MAOMAO; HUANG YANQUN; LAN HONGYUN; HE XUEWEI; LING MEIZHEN
- ↑ Ujihara K, Mori T, Iwasaki T, Sugano M, Shono Y, Matsuo N (2004) Biosci Biotechnol Biochem 68:170–174
- ↑ Crombie L, Doherty CF, Pattenden G (1970) J Chem Soc C 8:1076–1080
- ↑ Maund, S.J. et al. (2011). Ecotoxicology of Synthetic Pyrethroids. In: Matsuo, N., Mori, T. (eds) Pyrethroids. Topics in Current Chemistry, vol 314. Springer, Berlin, Heidelberg. https://doi.org/10.1007/128_2011_260
- ↑ Shamim MT, Hoffmann MD, Melendez J, Ruhman MA (2008) Ecological risk characteriza- tion for the synthetic pyrethroids. In: Gan J, Spurlock F, Hendley P, Weston DP (eds) Synthetic pyrethroids. Occurrence and behavior in aquatic environments, Chap 13. ACS Symposium Series 991, American Chemical Society, Washington DC, pp 257–309
Liens externes
- Portail de la chimie
- Portail de la protection des cultures