Cycle de Born-Haber
Le cycle de Born-Haber, ou cycle de Born-Fajans-Haber, est une technique permettant de calculer l'énergie réticulaire (enthalpie de cristallisation) d'un cristal ionique. Il est issu des travaux du physicien allemand Max Born, du chimiste allemand Fritz Haber et du physico-chimiste polonais Kazimierz Fajans.
La stabilité d'un cristal est caractérisée par son énergie réticulaire . Cette dernière représente la quantité d'énergie nécessaire pour décomposer une mole d'un solide cristallisé en ses ions constituants en phase gazeuse. Plus est importante, plus le solide est stable. Dans le diagramme ci-dessous, l'énergie réticulaire est notée .
Exemple de calcul
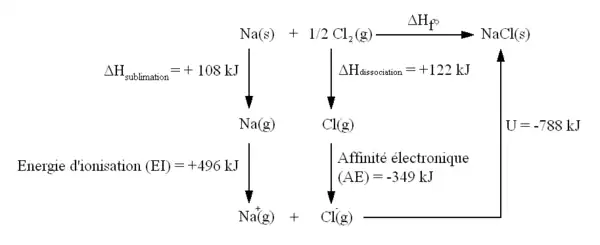
L'exemple classique est celui du réseau de chlorure de sodium NaCl. L'énergie réticulaire correspond à l'énergie libérée lors de la formation du réseau de NaCl solide à partir des ions Na+ et Cl- à l'état gazeux selon la réaction :
La réaction s'effectue à pression et température constantes, elle est ici considérée à la pression standard de 1 bar. Les étapes intermédiaires considérées pour cette réaction sont :
- 1a - Le sodium gazeux ionisé Na+(g) gagne un électron pour former le sodium monoatomique gazeux Na(g) : l'énergie nécessaire est l'opposé de l'enthalpie d'ionisation : = −496 kJ mol−1.
- 2a - Le sodium monoatomique gazeux Na(g) devient le sodium solide Na(s) : l'énergie nécessaire est l'opposé de l'enthalpie de sublimation : = −108 kJ mol−1.
- 1b - Le chlore monoatomique gazeux ionisé Cl-(g) perd un électron pour former le chlore monoatomique gazeux Cl(g) : l'énergie nécessaire est l'opposé de l'affinité électronique : = 349 kJ mol−1.
- 2b - Le chlore monoatomique gazeux Cl(g) s'associe pour former le dichlore gazeux Cl2(g) selon la réaction Cl(g) → 1⁄2 Cl2(g) : l'énergie nécessaire est l'opposé de l'enthalpie de dissociation : = −122 kJ mol−1.
- 3- Le sodium solide Na(s) et le dichlore gazeux Cl2(g) forment le chlorure de sodium solide selon la réaction Na(s) + 1⁄2 Cl2(g) → NaCl(s) : l'énergie nécessaire est l'enthalpie standard de formation = −411 kJ mol−1.
Le bilan énergétique du cycle s'écrit finalement :
- = −788 kJ mol−1.
Le cycle de Haber est principalement utilisé pour estimer l'enthalpie standard de formation (ici celle du chlorure de sodium solide NaCl(s)) à partir des autres données, plus accessibles :
Notes et références
- Peter William Atkins (trad. Monique Mottet), Éléments de chimie physique [« Physical Chemistry »], De Boeck Supérieur, , 512 p. (ISBN 978-2-7445-0010-7, lire en ligne), p. 367-368.
- Hubert H. Girault, Électrochimie physique et analytique, EPFL Press, , 572 p. (ISBN 9782880746735, lire en ligne), p. 128-134.
Liens externes
- Portail de la physique
- Portail de la chimie