Microscopie à expansion
La microscopie à expansion (ou microscopie d'expansion) ou ExM (pour Expansion microscopy) est un outil de préparation d'échantillons pour les échantillons biologiques qui permet aux chercheurs d'identifier de petites structures en les dilatant à l'aide d'un système polymère[1].
Le principe est d'introduire un réseau polymère dans des échantillons cellulaires ou tissulaires, puis d'étendre physiquement ce réseau polymère en utilisant des réactions chimiques pour augmenter la taille des structures biologiques. Entre autres avantages, ExM permet d'imager ces petites structures avec une gamme plus large de techniques de microscopie. Cette idée a été proposée pour la première fois dans un article de 2015 de Fei Chen, Paul W. Tillberg et Edward Boyden[2]. Les recherches actuelles permettent d'agrandir des échantillons jusqu'à 16 fois[3]. Ceci s'est avérée utile dans divers contextes de laboratoire, comme l'analyse de molécules biologiques. ExM permet aux chercheurs d'utiliser un équipement standard pour identifier les petites structures, mais nécessite des procédures strictes pour garantir des résultats clairs.
Principes
But
Les limites de résolution de la microscopie optique traditionnelle l'empêchent de distinguer faiblement certaines petites structures importantes pour la fonction biologique, qui doivent alors être observées via une technique à plus haute résolution, telle que la microscopie électronique. Par exemple, les vésicules synaptiques ont un diamètre de 40 à 50 nanomètres, ce qui est inférieur à la limite de résolution couramment citée de 200 nanomètres pour la microscopie optique[4].
La microscopie d'expansion, sans nécessiter d'équipement spécialisé ou coûteux[5], résout ce problème en agrandissant l'échantillon de tissu. Elle permet en outre de colorer et visualiser des molécules particulières dans l'échantillon, telles que des protéines spécifiques ou de l'ARN, pour identifier leur densité et leur distribution par rapport aux structures biologiques d'intérêt.
Étapes
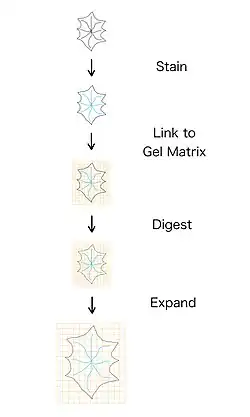
Le protocole, présente des exigences en matière de gélification et d'expansion. Les étapes sont la coloration, la liaison, la digestion et l'expansion[5].
Le processus de coloration utilise des fluorophores capables de se fixer au polymère à l'étape suivante.
La liaison est le processus d'ajout d'un gel polymère aux cellules, qui perméabilise à travers la cellule ; et la liaison des fluorophores au gel.
La digestion consiste à ajouter une solution qui « digère » la cellule, en supprimant sa structure. Si cette étape échoue, le gel ne se dilatera pas uniformément car la cellule « résistera » à l'expansion, avec des fissures ou des fractures dans la cellule[6].
L'expansion physique du gel dans toutes les directions, cause aussi l'expansion des fluorophores attachés au gel.
Histoire
En 2015, trois chercheurs du Massachusetts Institute of Technology décrivent pour la première fois la microscopie à expansion comme une méthode permettant d'améliorer la résolution de la microscopie en gonflant un échantillon plutôt qu'en utilisant un équipement à plus haute résolution[2]. Depuis lors, l'ExM est de plus en plus utilisé, le plus souvent pour des échantillons biologiques.
En 2016, plusieurs articles ont décrit des solutions de contournement des limitations traditionnelle des sondes d'étiquetage d'ExM, proposant un moyen d'utiliser l'ExM avec des sondes de microscopie conventionnelles, permettant une utilisation plus large, incluant la microscopie à fluorescence des molécules d'ARN, ce qui a conduit à son tour au séquençage in situ spatialement précis, à savoir ExSeq (séquençage d'expansion), en 2021[7].
La microscopie d'expansion, ne permettait pas d'observer les plaques amyloïdes bêta liées à la maladie d'Alzheimer. Boyden a conçu le concept de « microscopie révélatrice d'expansion » en 2022, en ajoutant des marqueurs fluorescents après l'expansion plutôt qu'avant. Il a remplacé les enzymes par la chaleur. Cela a permis une expansion jusqu'à 20 fois, sans endommager les protéines, montrant les détails des synapses et, pour faire la lumière sur la maladie d'Alzheimer, révélant des spirales occasionnelles de protéines bêta-amyloïdes autour des axones, qui sont les parties filiformes des cellules nerveuses qui transportent les impulsions électriques[8].
Médecine, diagnostics
La microscopie à expansion peut par exemple être utilisé pour le diagnostic optique des maladies rénales à altérations minimales, des lésions néoplasiques mammaires précoces et pour repérer la différence entre les échantillons de tissus humains normaux et les échantillons de tissus cancéreux, permettant une utilisation de routine de la recherche clinique[9]. Appliquée sur des microréseaux contenant des échantillons de divers organes (sein, prostate, poumon, côlon, pancréas, rein, foie ovaire) normaux ou cancéreux, a permis le diagnostic et l'examen du réseau cellulaire des tissus malades. Cette imagerie révèle des caractéristiques de taille inférieure à la limite de diffraction des filaments intermédiaires de kératine et de vimentine, essentiels à la transition épithéliale mésenchymateuse, à la progression du cancer et à l'initiation des métastases[10].
Observer la morphologie à l'échelle nanométrique de biomolécules et d'échantillons provenant d'une large gamme d'organes humains devient possible à coûts moins élevés.
Neuroscience
L'ExM permet d'agrandir des échantillons de circuits neuronaux et d'observer et cartographier plus facilement les synapses, cellules et des circuits neuronaux. Les biomolécules, telles que les protéines et les acides nucléiques, sont ancrées au polymère, qui est ensuite gonflé afin de dilater les biomolécules. En raison de la distance accrue entre les biomolécules, les microscopes ordinaires peuvent alors réaliser des images à résolution nanométrique. Grâce à l'utilisation de la technique ExM, les neuroscientifiques peuvent plus facilement cartographier les images[11].
Sous-ensembles
Avec le développement de la microscopie à expansion, les scientifiques ont commencé à créer des sous-ensembles de la technique, notamment la microscopie à expansion à balayage Joule, ou SJEM, qui est une technique d'imagerie thermique mesurant la dilatation thermique des éléments chauffés par effet Joule. L'un des plus grands avantages du SJEM par rapport aux anciennes techniques d'imagerie thermique submicronique est qu'il ne nécessite pas la nanofabrication de sondes spécialisées. Au contraire, le SJEM ne nécessite qu'un microscope à force atomique standard et une électronique simple[12].
Avantages
L'avantage le plus cité est que l'ExM ne nécessite pas d'équipement optique plus puissant pour réaliser une imagerie haute résolution.
En agrandissant l'échantillon physique, l'ExM évite aux chercheurs d'avoir à acheter un équipement de microscopie coûteux, comme des microscopes électroniques pour des études de super-résolution. En élargissant l'échantillon, il devient plus facile à examiner car les structures plus grandes peuvent alors être examinées à l'aide de techniques de microscopie traditionnelles, telles que la microscopie optique.
Limites
Chacune des quatre étapes de préparation d'ExM doit être parfaitement exécutée et terminée, sinon la cellule ne produira pas une coloration brillante et claire, ou il y aura rupture de la cellule ou une expansion inégale, déformant l'image.
L'ExM rencontre deux autres limitations[13] :
- difficultés dans les procédures utilisant des marqueurs fluorophores, car la polymérisation du gel peut blanchir ces fluorophores, les rendant inutiles. Certains, comme Alexa 488 et Atto 565, restent efficaces après polymérisation, mais leur efficacité est fortement diminuée, jusqu'à environ 50 %.
- conjuguer de l'ADN avec un autre anticorps est souvent coûteux et difficile, mais parfois rendue possible, après l'expansion, alors que le tissu est beaucoup moins dense et permet souvent une meilleure réception des anticorps fluorescents.
Références
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Expansion microscopy » (voir la liste des auteurs).
- ↑ (en-US) John Markoff, « Expansion Microscopy Stretches Limits of Conventional Microscopes », sur The New York Times, (ISSN 0362-4331, consulté le ).
- 1 2 Chen, Tillberg et Boyden 2015.
- ↑ (en) « Larger than Life: Monique Copeland and Paul Tillberg Explain Expansion Microscopy | Janelia Research Campus », janelia.org (consulté le ).
- ↑ (en) Tom Fagan, « Kiss and Tell—STED Microscopy Resolves Vesicle Recycling Question », AlzForum (consulté le ).
- 1 2 (en) « Expansion microscopy with conventional antibodies and fluorescent proteins », Nature Methods, vol. 13, no 6, , p. 485–8 (PMID 27064647, PMCID 4929147, DOI 10.1038/nmeth.3833).
- ↑ Wassie, Zhao et Boyden 2019.
- ↑ (en) Shahar Alon, Daniel R. Goodwin, Anubhav Sinha et Asmamaw T. Wassie, « Expansion sequencing: Spatially precise in situ transcriptomics in intact biological systems », Science, vol. 371, no 6528, , eaax2656 (ISSN 0036-8075, PMID 33509999, PMCID 7900882, DOI 10.1126/science.aax2656).
- ↑ (en) « Making the invisible visible », sur The Economist (ISSN 0013-0613, consulté le ).
- ↑ (en) « Synthetic Neurobiology Group: Ed Boyden, Principal Investigator », syntheticneurobiology.org (consulté le ).
- ↑ (en) « Nanoscale imaging of clinical specimens using pathology-optimized expansion microscopy », Nature Biotechnology, vol. 35, no 8, , p. 757–764 (PMID 28714966, PMCID 5548617, DOI 10.1038/nbt.3892).
- ↑ Karagiannis et Boyden 2018.
- ↑ (en) « Nanoscale Temperature Distributions Measured by Scanning Joule Expansion Microscopy », Journal of Heat Transfer, vol. 120, no 2, , p. 297–305 (DOI 10.1115/1.2824245).
- ↑ (en) I. Cho, J. Y. Seo et J. Chang, « Expansion microscopy », Journal of Microscopy, vol. 271, no 2, , p. 123–128 (ISSN 1365-2818, PMID 29782656, DOI 10.1111/jmi.12712).
Voir aussi
Bibliographie
![]() : document utilisé comme source pour la rédaction de cet article.
: document utilisé comme source pour la rédaction de cet article.
En français
- [Larousserie 2024] David Larousserie, « La révolution de la microscopie par expansion »
 , sur lemonde.fr, .
, sur lemonde.fr, .
En anglais
- [Chen, Tillberg et Boyden 2015] (en) Fei Chen, Paul W. Tillberg et Edward S. Boyden, « Expansion microscopy », Science, vol. 347, no 6221, , p. 543-548 (ISSN 0036-8075, e-ISSN 1095-9203, PMID 25592419, PMCID 4312537, DOI 10.1126/science.1260088, Bibcode 2015Sci...347..543C, lire en ligne [PDF]).

- [Gallagher et Zhao 2021] (en) Brendan R. Gallagher et Yongxin Zhao, « Expansion microscopy: A powerful nanoscale imaging tool for neuroscientists », Neurobiology of Disease, vol. 154, , article no 105362 (ISSN 1095-953X, e-ISSN 0969-9961, PMID 33813047, PMCID PMC8600979, DOI 10.1016/j.nbd.2021.105362).
- [Karagiannis et Boyden 2018] (en) Emmanouil D. Karagiannis et Edward S. Boyden, « Expansion microscopy: development and neuroscience applications », Current Opinion in Neurobiology, vol. 50, , p. 56-63 (ISSN 0959-4388, e-ISSN 1873-6882, PMID 29316506, PMCID PMC5984670, DOI 10.1016/j.conb.2017.12.012
 , S2CID 4908781, lire en ligne [PDF]).
, S2CID 4908781, lire en ligne [PDF]). 
- [Wassie, Zhao et Boyden 2019] (en) Asmamaw T. Wassie, Yongxin Zhao et Edward S. Boyden, « Expansion microscopy: principles and uses in biological research », Nature Methods, vol. 16, no 1, , p. 33-41 (ISSN 1548-7091, e-ISSN 1548-7105, PMID 30573813, PMCID PMC6373868, DOI 10.1038/s41592-018-0219-4
 , lire en ligne [PDF]).
, lire en ligne [PDF]). 
- [Wen et al. 2023] (en) Gang Wen, Volker Leen, Taoufik Rohand, Markus Sauer et Jhan Hofkens, « Current Progress in Expansion Microscopy: Chemical Strategies and Applications », Chemical Reviews, vol. 123, no 6, , p. 3299-3323 (ISSN 0009-2665, e-ISSN 1520-6890, PMID 36881995, DOI 10.1021/acs.chemrev.2c00711
 , S2CID 257404259, lire en ligne [PDF]).
, S2CID 257404259, lire en ligne [PDF]). - [Zhuang et Shi 2023] (en) Yinyin Zhuang et Xiaoyu Shi, « Expansion microscopy: A chemical approach for super-resolution microscopy », Current Opinion in Structural Biology, vol. 81, , article no 102614 (ISSN 0959-440X, e-ISSN 1879-033X, PMID 37253290, PMCID PMC11103276, DOI 10.1016/j.sbi.2023.102614).
Articles connexes
- Portail de la physique