Phénylméthanediol
| Phénylméthanediol | |
| |
| Identification | |
|---|---|
| Nom UICPA | Phénylméthanediol |
| Nom systématique | Phénylméthanediol |
| No CAS | |
| PubChem | 427890 |
| SMILES | |
| InChI | |
| Propriétés chimiques | |
| Formule | C7H8O2 [Isomères] |
| Masse molaire[1] | 124,137 2 ± 0,006 8 g/mol C 67,73 %, H 6,5 %, O 25,78 %, |
| Unités du SI et CNTP, sauf indication contraire. | |
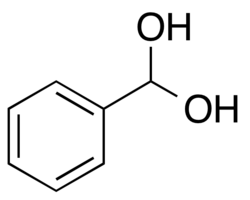
Le phénylméthanediol est composé aromatique constitué d'un cycle benzénique, substitué par un groupe méthyle porteur d'une fonction diol géminal. C'est la forme hydratée du benzaldéhyde, un intermédiaire réactionnel de courte durée de vie dans certaines réactions, par exemple l'oxydation du toluène[2] ou du benzaldéhyde[3], ou encore la réduction de l'acide benzoïque[4].
Notes et références
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Phenylmethanediol » (voir la liste des auteurs).
- ↑ Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- ↑ Pritchard, Huw O., « On the atmospheric oxidation of liquid toluene », Physical Chemistry Chemical Physics, vol. 8, no 39, , p. 4559–4562 (PMID 17047753, DOI 10.1039/b608510e, Bibcode 2006PCCP....8.4559P)
- ↑ Nigam, S. K.; Khan, M. U.; Tiwari, Saras; Dwivedi, H. P.; Singh, P. K., « Kinetics and mechanism of oxidation of benzaldehyde and substituted benzaldehyde by N-chlorosaccharin », Asian Journal of Chemistry, vol. 16, no 2, , p. 761–766
- ↑ Cheng, Po-Chung; Nonaka, Tsutomu, « Kinetic study of the electroreduction of benzoic acid », Bulletin of the Chemical Society of Japan, vol. 68, no 1, , p. 378–84 (DOI 10.1246/bcsj.68.378)
- Portail de la chimie