Violet de méthyle
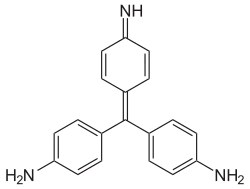
Les violets de méthyle sont des mélanges de composés organiques à structure amino-triarylméthane[1] utilisés comme colorants. Ils sont référencés dans le Colour Index sous le numéro C.I. 42535 avec l'appellation « C.I. Basic Violet 1 » et dérivent de la pararosaniline (en), elle-même apparentée aux fuchsines.
Plus précisément, ce sont des mélanges de dérivés N-méthylés de la pararosaniline obtenus en ajoutant un à deux groupements méthyle (–CH3) sur chacun des atomes d'azote de la molécule de pararosaniline. Leur définition exacte varie selon les sources, comprenant toujours les dérivés penta- (5 méthyles) et hexaméthylés (6 méthyles) et pouvant englober[2],[3], ou non[1], l'un des deux isomères du dérivé tétraméthylé (la N,N,N',N"-tétraméthyl-pararosaniline : 4 méthyles, un seul atome d'azote en portant deux).
Variétés

Des lettres ont été ajoutées après les mots « violet de méthyle » pour désigner la teinte des différentes variétés, corrélée au degré de méthylation de ses composants : elle varie du rougeâtre (lettre R, voire 2R, pour Red) lorsque les moins méthylés dominent, au bleu de plus en plus foncé (B pour Blue, puis 2B, 3B etc.) à mesure que la proportion de dérivés plus méthylés augmente dans le mélange[1].
Violet de méthyle 10B
Le terme « violet de méthyle 10B » fait référence de manière univoque au dérivé hexaméthylé (càd. le plus méthylé qui soit) de la pararosaniline, plus connu sous le nom de violet cristallisé (en anglais crystal violet)[4],[5],[6].
Autres violets de méthyle
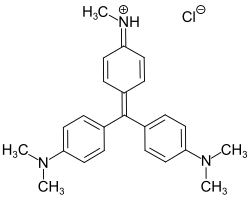
Le terme « violet de méthyle 2B » est utilisé dans certaines sources pour désigner le dérivé pentaméthylé de la pararosaniline[6],[7].
La dénomination « violet de méthyle 6B » est plus équivoque. Elle a pu être utilisée pour désigner le composé pentaméthylé précédent[1],[8], mais selon d'autres sources c'est seulement le nom d'un mélange plus sombre que le 2B et plus clair que le 10B[9].
L'analyse chimique semble indiquer que les substances vendues sous le nom de « violet de méthyle » sont toutes des mélanges de dérivés homologues[1]. Ils sont très proches du violet de gentiane, dénomination historique de mélanges des mêmes dérivés méthylés de pararosaniline.
Applications
De nombreuses applications du violet de méthyle sont décrites dans la littérature, sans que la nature chimique exacte de la substance étudiée soit toujours précisée.
Microbiologie
Dans une étude portant sur le mécanisme de la coloration de Gram, le violet de méthyle (variété « B » de Grübler) a été décrit comme un substitut acceptable au violet cristallisé pour la coloration primaire[10]. Une coloration des Spirochètes à base de mercurochrome, de violet de méthyle et de solution de Lugol a été décrite[11]. Associé à la tartrazine, le violet de méthyle a été employé comme colorant pour la visualisation au microscope optique de Cryptosporidium spp. dans les prélèvements digestifs[12].
Le violet de méthyle a été utilisé comme ingrédient sélectif dans la composition de milieux de culture destinés à l'isolement d’Enterobacter spp.[13] et de K. pneumoniae[14],[15].
Biologie moléculaire et biochimie
Le violet de méthyle était utilisé pour détecter par un effet métachromatique les dépôts amyloïdes tissulaires dans les amyloses[16]. Bien qu'en perte de vitesse depuis l'introduction du rouge Congo, cette technique peu spécifique a été améliorée par adjonction d'une étape de différenciation au vert de méthyle purifié[17].
Une étude de biochimie analytique a exploité les interactions du violet de méthyle avec les acides nucléiques pour proposer une méthode de dosage des acides nucléiques totaux (ADN + ARN) par spectroscopie de diffusion Rayleigh[18].
Médecine
En ophtalmologie, des recherches précliniques ont été menées concernant l'utilisation potentielle du violet de méthyle pour teinter les tissus pré-rétiniens afin de faciliter la réalisation d'une vitrectomie (chromovitrectomie). Dans une étude animale, le violet de méthyle administré par voie intravitréenne à des lapins a été considéré comme une option sûre et efficace[19]. Une étude antérieure avait mis en évidence des lésions histologiques de la rétine à la suite d'injections similaires effectuées sur des porcs[20].
Le violet de méthyle administré par injection rétrograde dans le canal parotidien (Sténon) a été utilisé comme agent sclérosant dans une petite série de patients atteints de parotidite obstructive chronique[21].
Autres applications
Des systèmes électrochimiques mettant en jeu le violet de méthyle ont été décrits : pile à combustible biologique[22], électrode analytique de dosage du chrome(III)[23].
Toxicité
Animale et microbiologique
Une toxicité subaiguë significative a été observée chez l'animal par voie intraveineuse et rapportée à la formation de précipités avec les protéines plasmatiques responsables d'embolies pulmonaires[24].
Un effet mutagène dose-dépendant a été observé chez le phage T4[25] alors qu'une étude sur des cellules procaryotes (S. typhimurium) et eucaryotes (S. cerevisiae) n'avait pas démontré de mutagenèse significative[26]. Une interaction génotoxique par intercalation du violet de méthyle dans de l'ADN animal (thymus de veau) a été démontrée in vitro[27].
Environnementale
Notes et références
- 1 2 3 4 5 Horobin RW & Kiernan JA (eds.) Conn's biological stains. A handbook of dyes, stains and fluorochromes for use in biology and medicine. New York : Taylor & Francis, 10th ed, 2002, p. 192. (ISBN 1 85996099 5)
- ↑ Society of dyers & colourists (ed.) Colour Index, vol. 4. Bradford & London : Lund Humphries, 3rd ed, 1971, p. 4390. (ISBN 0901956066)
- ↑ Gessner T & Mayer U (2000) « Triarylmethane and diarylmethane dyes » in: Ullmann's Encyclopedia of Industrial Chemistry (ISBN 9783527306732) DOI 10.1002/14356007.a27_179
- ↑ Horobin RW & Kiernan JA (eds.) Conn's biological stains. A handbook of dyes, stains and fluorochromes for use in biology and medicine. New York : Taylor & Francis, 10th ed, 2002, p. 193. (ISBN 1 85996099 5)
- ↑ Cooksey CJ « Quirks of dye nomenclature. 7. Gentian violet and other violets » Biotech Histochem. 2017;92(2):134-140. DOI 10.1080/10520295.2017.1286038
- 1 2 « Methyl violet 2B (Methyl violet) » in: Sabnis RW. Handbook of biological dyes and stains. Synthesis and industrial applications. Hoboken, New Jersey : John Wiley & Sons, Inc., 2010, p. 309. (ISBN 978-0-470-40753-0)
- ↑ Maley AM & Arbiser JL « Gentian violet: a 19th century drug re-emerges in the 21st century » Exp Dermatol. 2015;22(12):775-780. DOI 10.1111/exd.12257
- ↑ Bouasla C et al. « Degradation of methyl violet 6B dye by the Fenton process » Desalination 2010;254(1-3):35-41. DOI 10.1016/j.desal.2009.12.017
- ↑ Methyl violet 2B,6B sur le site StainsFile (consulté le 15/05/2025).
- ↑ Bartholomew JW & Mittwer T « The mechanism of the Gram reaction I. The specificity of the primary dye » 1950;25(2):103-110. DOI 10.3109/10520295009110965
- ↑ Vago SC « Intensified form of the mercurochrome-methyl-violet stain for spirochetes » Stain Technol. 1953;28(2):87-88. DOI 10.3109/10520295309105105
- ↑ Milácek P & Vítovec J « Differential staining of cryptosporidia by aniline-carbol-methyl violet and tartrazine in smears from feces and scrapings of intestinal mucosa » Folia Parasitol (Praha). 1985;32(1):50. Accès libre.
- ↑ Fung DYC & Miller RD « Effects of dyes on bacterial growth » Appl Microbiol. 1973;25(5):793-799. DOI 10.1128/am.25.5.793-799.1973
- ↑ Campbell LM & Roth IL « Methyl violet: a selective sgent for differentiation of Klebsiella pneumoniae from Enterobacter aerogenes and other Gram-negative organisms » Appl Microbiol. 1975;30(2):258-261. DOI 10.1128/am.30.2.258-261.1975
- ↑ Campbell LM & Roth IL « Evaluation of double violet agar in the isolation of Klebsiella pneumoniae from river water » Appl Environ Microbiol. 1976;31(2):213-215. DOI 10.1128/aem.31.2.213-215.1976
- ↑ Suvarna KS et al. (eds.) Bancroft's theory and practice of histological techniques. Elsevier, 8th ed, 2019, p. 242. (ISBN 978-0-7020-6864-5)
- ↑ Bancroft JD « Methyl green as a differentiator and counterstain in the methyl violet technique for demonstration of amyloid in fresh cryostat sections » Stain Technol. 1963;38(6):336-337. DOI 10.3109/10520296309061198
- ↑ Liu Y et al. « Rayleigh light scattering study on the reaction of nucleic acids and methyl violet » Anal Biochem. 1999;268(2):187-192. DOI 10.1006/abio.1998.3012
- ↑ Badaro E et al. « Investigation of new dyes for chromovitrectomy: preclinical biocompatibility of trisodium, orangell and methyl violet » Int J Retina Vitreous. 2015;1(1). DOI 10.1186/s40942-015-0003-x
- ↑ Rodrigues EB et al. « Ability of new vital dyes to stain intraocular membranes and tissues in ocular surgery » Am J Ophtalmol. 2010;149(2):265-277. DOI 10.1016/j.ajo.2009.08.020
- ↑ Wang S et al. « Gland atrophy following retrograde injection of methyl violet as a treatment in chronic obstructive parotitis » Oral Surg Oral Med Oral Pathol Oral Radiol Endod. 1998;85(3):276-281. DOI 10.1016/s1079-2104(98)90008-7
- ↑ Sun C et al. « A biofuel cell of (methyl violet/AuNPs)25/FTO photoanode and bilirubin oxidase/CuCo2O4 bio-photocathode inspired by the photoelectrochemistry activities of fluorescent materials/molecules » RSC Adv. 2025;15(1):665-673. DOI 10.1039/d4ra08117j
- ↑ Kazemi SY et al. « Optimization of a new polymeric chromium (III) membrane electrode based on methyl violet by using experimental design » Talanta 2010;81(4-5):1681-1687. DOI 10.1016/j.talanta.2010.03.012
- ↑ Cutlip RC & Monlux WS « Experimental crystal violet and methyl violet poisoning in dogs and cattle » Can J Comp Med Vet Sci. 1967;31(3):80-84.
- ↑ Kvelland I « The mutagenic effect of methyl violet in phage T4D » Hereditas 1983;98(1):145-147. DOI 10.1111/j.1601-5223.1983.tb00588.x
- ↑ Shahin MM & von Borstel RC « Comparisons of mutation induction in reversion systems of Saccharomyces cerevisiae and Salmonella typhimurium » Mutat Res. 1978;53(1):1-10. DOI 10.1016/0165-1161(78)90374-6
- ↑ Chi Z et al. « Study on the genotoxic interaction of methyl violet with calf thymus DNA » Appl Spectrosc. 2009;63(12):1331-1335. DOI 10.1366/000370209790109085
Voir aussi
Liens externes
- Portail de la chimie
- Portail de la biochimie
- Portail de la microbiologie