Xantphos
| Xantphos | ||

| ||
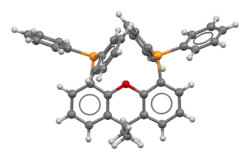 | ||
| Représentation 2D et 3D du Xantphos (Ph représente les groupes phényl) | ||
| Identification | ||
|---|---|---|
| Nom UICPA | (9,9-Dimethyl-9H-xanthene-4,5-diyl)bis(diphenylphosphane) | |
| Synonymes |
4,5-Bis(diphenylphosphino)-9,9-dimethylxanthene |
|
| No CAS | ||
| No ECHA | 100.118.008 | |
| PubChem | ||
| SMILES | ||
| InChI | ||
| Apparence | Solide incolore | |
| Propriétés chimiques | ||
| Formule | C39H32OP2 |
|
| Masse molaire[1] | 578,618 3 ± 0,033 7 g/mol C 80,95 %, H 5,57 %, O 2,77 %, P 10,71 %, |
|
| Propriétés physiques | ||
| T° fusion | 224 à 228 °C (435 à 442 °F; 497 à 501 K) | |
| Solubilité | Solvants organiques | |
| Masse volumique | 1,34 g/ml | |
| Précautions | ||
| SGH[2] | ||
 Danger |
||
| Unités du SI et CNTP, sauf indication contraire. | ||
Le xantphos est un composé organophosphoré dérivé de l'hétérocycle xanthène. Il est utilisé comme ligand diphosphine bidente et se distingue par son angle de morsure particulièrement large (108°)[3]. De tels ligands sont utiles dans l'hydroformylation des alcènes[4]. Illustrant son grand angle de morsure, il forme à la fois des adduits cis et trans du chlorure de platine (II). Dans ce dernier contexte, le xantphos est classé comme un ligand trans-transversal . Un ligand bidente apparenté ayant un angle de morsure (bite-angle) plus grand est le spanphos.
Ce ligand est préparé par lithiation doublement dirigée du 9,9-diméthylxanthène avec du sec-Butyllithium suivi d'un traitement avec de la chlorodiphénylphosphine[5].
Références
- ↑ Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- ↑ Fiche de sécurité fournie par Sigma-Aldrich, consultée le .
- ↑ Birkholz, Freixa et van Leeuwen, « Bite angle effects of diphosphines in C–C and C–X bond forming cross coupling reactions », Chemical Society Reviews, vol. 38, no 4, , p. 1099–118 (PMID 19421583, DOI 10.1039/B806211K)
- ↑ Piet W. N. M. van Leeuwen, Paul C. J. Kamer, Joost N. H. Reek, and Peter Dierkes, « Ligand Bite Angle Effects in Metal-catalyzed C-C Bond Formation », Chemical Reviews, vol. 100, no 8, , p. 2741–2769 (PMID 11749304, DOI 10.1021/cr9902704)
- ↑ Mirko Kranenburg, Yuri E. M. van der Burgt, Paul C. J. Kamer, Piet W. N. M. van Leeuwen, Kees Goubitz, and Jan Fraanje, « New Diphosphine Ligands Based on Heterocyclic Aromatics Inducing Very High Regioselectivity in Rhodium-Catalyzed Hydroformylation: Effect of the Bite Angle », Organometallics, vol. 14, no 6, , p. 3081–3089 (DOI 10.1021/om00006a057, S2CID 53053952, lire en ligne)
- Portail de la chimie